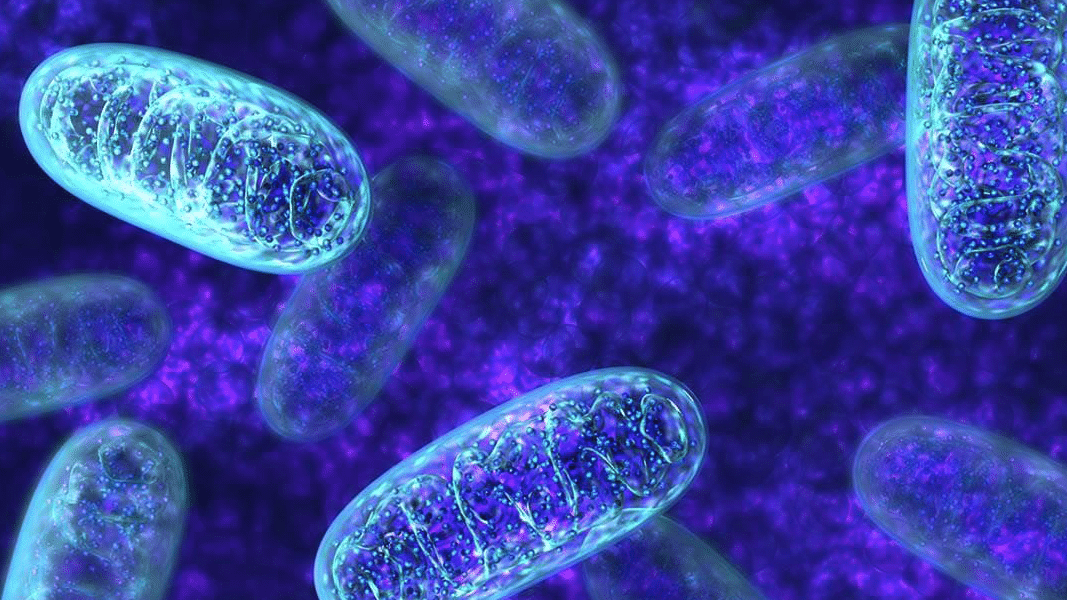
En 2012, científicos franceses reportaron la presencia de receptores cannabinoides en las membranas de la mitocondria, el organelo generador de energía dentro de las células. Este descubrimiento sentó las bases para investigaciones subsecuentes en el rol del sistema endocannabinoide en regular la actividad mitocondrial, la cual es crítica en la función celular. Los defectos en la mitocondria han sido asociados a un amplio margen de desórdenes neurodegenerativos, autoinmunes y metabólicos –Alzheimer, esquizofrenia, autismo, cáncer, epilepsia, diabetes, enfermedades cardiovasculares y neuromusculares, y más.
Un creciente cuerpo de datos científicos indica que el cannabidiol (CBD) y el tetrahidrocannabinol (THC), dos componentes clave de la planta de Cannabis, pueden afectar la mitocondria, directa e indirectamente. Resulta que muchos procesos biológicos que involucran a la mitocondria – incluyendo la homeostasis energética, la emisión de neurotransmisores y el estrés oxidativo – son modulados por cannabinoides endógenos y exógenos.
Pero la investigación con cannabinoides a menudo parece estar plagada con contradicciones. Los cannabinoides son notorios (en la ciencia y la experiencia) por ejercer efectos opuestos en diferentes situaciones. ¿Cómo el CBD y el THC son capaces de balancear el exceso fisiológico y también la deficiencia? ¿Por qué una pequeña dosis de Cannabis estimula mientras que una dosis mayor tiende a sedar? ¿Cómo es posible que los compuestos cannabinoides puedan destruir células cancerosas sin afectar a las células saludables? Examinar el rol de la mitocondria arroja luces sobre estas preguntas y otros aspectos perplejos del sistema endocannabinoide.
¿Qué son las mitocondrias?
Las mitocondrias son adaptadores universales de energía que existen en las células de cada organismo multicelular, incluyendo a los humanos. El número de mitocondrias en una célula individual puede variar grandemente dependiendo del organismo y el tipo de tejido. (Todas las células humanas, excepto los glóbulos rojos, contienen mitocondrias.) Una de las principales funciones de la mitocondria es tomar moléculas de alta energía – como los azúcares y los aminoácidos – y convertirlas en una forma de energía llamada Adenosín Trifosfato (ATP), la cual puede ser usada por la célula. Para la célula, el ATP es como la batería.
El proceso de extraer pequeños paquetes de energía de moléculas de alta energía puede ser muy peligroso. Imagine tratar de encender un automóvil simplemente prendiendo en llamas el tanque del combustible. Una célula no puede manejar el equivalente microscópico de una explosión, por lo tanto la célula debe usar la refinación para aprovechar esta energía. Los electrones individuales son extraídos de moléculas de alta energía por un proceso llamado Respiración Celular y su energía es gradualmente emitida.
Esta emisión gradual de electrones individuales le permite a la célula sintetizar ATP de sus precursores, el adenosín difostato (ADP) y el fosfato inorgánico (Pi). La fractura de ATP hacia sus precursores ADP y Pi emite una pequeña cantidad de energía la cual le da poder a las proteínas que permiten que cada célula funcione y se comunique. El ATP es la principal fuente de energía de la mayoría de las funciones celulares. Aunque es comúnmente referida como el centro de poder de la célula, las mitocondrias también están involucradas en otras funciones relacionadas con el metabolismo, pero la meta es siempre la misma –homeostasis, el mantenimiento de un medio interno estable a pesar de fluctuaciones externas.
Simbiosis
Originalmente, las mitocondrias estaban separadas de otras células. En cierto punto, entre 1.500 y 2.000 años atrás, una célula engulló un precursor evolutivo de una mitocondria. Pero en lugar de digerir la mitocondria, las dos entidades vivientes formaron una relación simbiótica. La célula huésped proporcionaría nutrientes y un lugar seguro para que la mitocondria existiera, y la mitocondria realizaría el peligroso proceso de respiración celular, dando al huésped una forma de energía más utilizable. El resultado fue tan evolutivamente fundamental que esta relación simbiótica precedió a la aparición de organismos multicelulares. Todas las plantas, animales y hongos están dotados de mitocondrias.
Esta teoría de cómo dos diferentes sistemas vivos auto organizados comenzó a colaborar simbióticamente es apoyada por el hecho de que las mitocondrias han conservado su propio genoma que está separado del ADN de la célula huésped. Las mitocondrias y la célula huésped se replican independientemente; También tienen membranas celulares separadas. Se cree que otros dos organelos se han desarrollado de manera similar: el cloroplasto, que permite la fotosíntesis en las plantas, y el núcleo, que contiene el ADN celular y actúa como una especie de coordinador de la célula.
Las enfermedades mitocondriales pueden ser causadas por mutaciones heredadas en el ADN mitocondrial o defectos en los genes nucleares que codifican las proteínas encargadas de regular la división mitocondrial y la replicación del ADN. Los trastornos mitocondriales también pueden desarrollarse debido a los efectos adversos de los medicamentos, las infecciones, las toxinas ambientales o los hábitos de vida poco saludables. Las enfermedades mitocondriales son más graves cuando las mitocondrias defectuosas están presentes en el tejido muscular, cerebral o nervioso, ya que estas células requieren más energía (y por lo tanto más actividad mitocondrial).
Radicales libres y fitocannabinoides
Enemigos y Potenciadores de las Mitocondrias
Las deficiencias de aceites omega 3 y probióticos, bajos niveles de vitamina D y otros desequilibrios nutricionales contribuyen a la disfunción mitocondrial. Lo mismo ocurre con muchos medicamentos recetados, edulcorantes artificiales y aditivos tóxicos para alimentos. Originado en las malas dietas y pobres hábitos de vida, el cáncer puede ser pensado como un trastorno metabólico mitocondrial. El azúcar alimenta el cáncer, mientras que las grasas saturadas lo matan de hambre.
Los antioxidantes encontrados en muchas plantas han sido promovidos como suplementos alimenticios naturales para minimizar el daño de los radicales libres. Un antioxidante parecido a una vitamina conocido como CoQ10 o ubiquinona facilita la función mitocondrial. Los alimentos ricos en CoQ10 incluyen brócoli, coliflor, semillas de sésamo, pescado aceitoso, pollo y carne de vaca alimentada con pasto. Además de una dieta saludable, el ejercicio es una excelente manera de estimular la reparación y la regeneración mitocondrial. Varios estudios científicos también muestran que la terapia de láser de bajo nivel puede acelerar el proceso de curación mediante el desencadenamiento de la actividad mitocondrial y la síntesis de ATP. – Proyecto CBD
Aunque las mitocondrias permiten acceder a la energía a un ritmo moderado en cantidades relativamente pequeñas, el proceso de respiración celular, mediante el cual las células extraen energía de los nutrientes, aún puede ser dañino. Los electrones de alta energía descargan su energía en una multitud de complicados pasos, hasta que el electrón de menor energía es finalmente liberado sobre una molécula de oxígeno. Idealmente, la molécula de oxígeno interactuará con el hidrógeno y formará agua, que es muy estable.
Pero a veces el oxígeno ionizado, llamado superóxido, puede escapar, dando como resultado un estrés oxidativo. De forma similar, pueden formarse y escapar otras moléculas inestables como peróxido y peróxido de hidrógeno. Estas moléculas renegadas, inestables, se llaman especies reactivas del oxígeno (ERO) o radicales libres. Los radicales libres causan daño al interactuar con el ADN, membranas celulares, proteínas y otros organelos.
Al neutralizar eficazmente los radicales libres y mitigar el estrés oxidativo, los antioxidantes confieren una amplia gama de beneficios terapéuticos, desde la ralentización del proceso de envejecimiento hasta la reducción del riesgo de daño al ADN relacionado con el cáncer. El THC y el CBD son ambos potentes antioxidantes, según el gobierno de los Estados Unidos, el cual presentó una patente sobre las propiedades antioxidantes y neuroprotectoras de los cannabinoides basado en investigaciones desde 1998. Esta patente subraya una de las grandes hipocresías de la política federal de drogas que sostiene falsamente que el cannabis no tiene valor médico.
Autofagia y apoptosis
El estrés oxidativo es un subproducto natural de la actividad mitocondrial. La creación del estrés oxidativo es necesaria para obtener energía y mantener la función celular. Inevitablemente, esto le pasará cuenta de cobro al organismo. Pero el daño oxidativo se puede reparar en cierta medida a través de un proceso adaptativo conocido como autofagia, por el cual las partes defectuosas de la célula – las proteínas mal plegadas o agregadas, las mitocondrias disfuncionales, etc. – son removidas y se reemplazan por componentes nuevos y mejores. La supervivencia celular depende de este mecanismo regenerativo continuo.
El estrés oxidativo no es exclusivamente malo. En niveles bajos, las especies de oxígeno reactivo actúan como moléculas de señalización. Las neuronas dañadas pueden deshacerse de sus mitocondrias desgastadas, que son interpretadas como un SOS por las células vecinas. Las células inmunes del cerebro, llamadas astrocitos, responden donando parte de sus propias mitocondrias a las neuronas afectadas. Las células pulmonares también pueden secretar mitocondrias saludables para que las células dañadas las utilicen. Bajos niveles de estrés oxidativo podrían estimular una limpieza celular necesaria, pero altos niveles de estrés oxidativo son una indicación de que algo va mal en la célula. Demasiado estrés oxidativo es una señal para que la célula se destruya a sí misma de una manera regulada, un proceso llamado apoptosis. Es como si hubiera un punto de inflexión cuando el daño oxidativo excede la capacidad de una célula para repararse a sí misma, por lo cual la célula sale del modo de supervivencia y comete suicidio por el bien del equipo. El destino de una célula – ya sea supervivencia a través de la autofagia o la muerte a través de apoptosis – depende del tipo de estrés al que se enfrenta y su duración.
La neurodegeneración relacionada con la edad
Mientras que el estrés oxidativo moderado puede ser utilizado por la célula, la desregulación del estrés oxidativo da lugar a la enfermedad. La interrupción de la delicada interacción entre la autofagia y la apoptosis permite que los radicales libres y las células dañadas se acumulen, lo que puede conducir a una amplia gama de patologías. La disfunción mitocondrial está implicada en prácticamente todas las enfermedades, especialmente la neurodegeneración relacionada con la edad. Dado que las neuronas utilizan una tremenda cantidad de energía para transmitir información a través del cuerpo, requieren mitocondrias altamente activas, lo que significa un mayor daño oxidativo. Esto lentamente conduce a una pérdida de funcionamiento y síntomas de deterioro relacionados con la edad.
De acuerdo con un informe de 2016 en Philosophical Transactions de la Royal Society de Londres: “Los cannabinoides como reguladores de la actividad mitocondrial, como antioxidantes y como moduladores de los procesos de depuración protegen las neuronas a nivel molecular… Los procesos neuroinflamatorios que contribuyen a la progresión del envejecimiento cerebral normal y a la patogénesis de las enfermedades neurodegenerativas son suprimidos por los cannabinoides, lo que sugiere que también pueden influir en el proceso de envejecimiento a nivel sistémico”.
El envejecimiento, la neurodegeneración, los trastornos metabólicos y los cánceres están todos relacionados con la actividad mitocondrial – o la falta de ella. (El descubrimiento de la mínima actividad mitocondrial en las células de cáncer, llamada efecto de Warburg, mereció a Otto Heinrich Warburg un premio Nobel en 1931.)1 Los estudios preclínicos indican que el THC puede inhibir la formación de placa amiloide en el cerebro, un sello distintivo de la demencia por Alzheimer, mediante el mejoramiento de la función mitocondrial. Y el CBD ha demostrado estimular la biogénesis mitocondrial y revertir los síntomas de la pérdida de memoria en animales. ¿Pero cómo los cannabinoides mejoran la función cognitiva? ¿Cómo interactúan con las mitocondrias y reducen la inflamación cerebral?
Mecanismos de acción – receptores y membranas
Existen tres maneras principales en que los cannabinoides vegetales y endógenos pueden modular directamente la función mitocondrial: 1) activando los receptores CB1 en la mitocondria; 2) perturbando la membrana mitocondrial; 3) uniéndose a otros receptores (no cannabinoides) en la superficie de las mitocondrias.
Receptores mitocondriales CB1. Incorporados en las membranas celulares, los receptores cannabinoides CB1 son los receptores acoplados a proteínas G más frecuentes en el cerebro humano y el sistema nervioso central. Se estima que el quince por ciento de todos los receptores CB1 en las neuronas existen en la mitocondria. En ciertos tipos de tejido muscular, la mitad de los receptores CB1 están localizados en la mitocondria. Para activar directamente un receptor CB1 mitocondrial, el THC debe penetrar en la membrana celular externa y ser acompañado a través del interior de la célula. Los receptores CB1 mitocondriales no son estructuralmente distintos de los prolíficos receptores CB1 que se envuelven alrededor de la superficie externa de la célula, pero sus efectos pueden ser muy diferentes. (Los interruptores de luz pueden parecer iguales de una habitación a otra, pero están conectados a diferentes circuitos en toda la casa y, por tanto, activar o desactivar el interruptor en diferentes lugares causa diferentes resultados). La ciencia preclínica sugiere que la activación de los receptores mitocondriales CB1 generalmente disminuye la actividad mitocondrial. Esto puede proteger a la célula del estrés oxidativo y prevenir la apoptosis, pero paradójicamente también puede causar la muerte celular en algunas condiciones.
Perturbación de la membrana. La membrana de las mitocondrias se compone principalmente de lípidos, como los ácidos grasos y el colesterol. Así como en la membrana celular externa, la concentración relativa de grasas de cadena corta y larga, grasas saturadas e insaturadas y colesterol influyen en muchos aspectos de la membrana mitocondrial. Los compuestos lipofílicos como los endocannabinoides y los cannabinoides vegetales también pueden fundirse en la membrana mitocondrial, cambiando su fluidez y permeabilidad. Las mitocondrias aprovechan la energía de los electrones mediante el uso de proteínas incrustadas en la membrana mitocondrial; La alteración de la fluidez de la membrana puede inhibir la capacidad de las mitocondrias para producir energía y permitir que los radicales libres escapen más fácilmente a la célula. Stephanie Seneff, investigadora principal del MIT, informa que el herbicida “Roundup” (Glifosato) de Monsanto interfiere con la producción de ATP al afectar de manera adversa la permeabilidad de la membrana mitocondrial.
Receptores no cannabinoides. El Cannabidiol no activa directamente los receptores mitocondriales CB1. En lugar de eso el CBD se une a diferentes receptores, incluyendo el intercambiador de sodio-calcio (NCX), en la superficie de las mitocondrias. La unión al NCX abre un canal iónico, y algunos iones, tales como los átomos de calcio cargados eléctricamente, fluyen desde altas concentraciones a bajas concentraciones. Diferentes niveles de iones de calcio tienen efectos diferentes.2 En condiciones de bajo estrés celular, caracterizado por un bajo nivel de calcio intracelular que rodea a las mitocondrias, el CBD aumentará el estrés al permitir que el calcio fluya fuera de ellas. Pero en condiciones de alto estrés, caracterizadas por abundante calcio intracelular, el CBD hará exactamente lo contrario, permitiendo el flujo de calcio desde el exterior al interior de la mitocondria (donde se almacena el calcio) abriendo el NCX. El flujo de calcio bidireccional regulado por el NCX es uno de los mecanismos por medio de los cuales el CBD facilita la homeostasis celular y la neuroprotección.
CBD, canales de calcio y homeostasis
Los cannabinoides son bien conocidos entre los científicos por su habilidad truculenta para ejercer efectos opuestos en diferentes situaciones. En las mitocondrias, la actividad cannabinoide es aún más complicada. En condiciones de bajo estrés, los cannabinoides a menudo aumentan la actividad mitocondrial y la respiración celular, provocando la reparación celular autofágica. Los cannabinoides también tamponarán las condiciones de alta tensión y protegerán las células al disminuir la actividad mitocondrial. Pero eso no es todo. La dependencia del estrés es en realidad trimodular: En condiciones de muy alto estrés – como las que a menudo se presentan en las células cancerosas – los endocannabinoides pueden crear un bucle de retroalimentación positiva, aumentando el estrés hasta el punto en que la célula sufre apoptosis. Los cannabinoides vegetales también pueden inducir la apoptosis en condiciones similares. La muerte de las células cancerosas promueve la homeostasis y la supervivencia del organismo en su conjunto3.
Las fluctuaciones del calcio y el estrés, la autofagia y la muerte celular y la restauración de la homeostasis a nivel celular son todos regulados por el CBD. Un informe de investigadores británicos en el Journal of Neuroscience (2009) señaló que “en condiciones patológicas que implican la disfunción mitocondrial y la desregulación del calcio [Ca (2+)], el CBD podría resultar beneficioso en la prevención de la señalización apoptósica a través de una restauración de la homeostasis del calcio”.
El examen del efecto del CBD sobre las mitocondrias arroja luz sobre cómo el cannabidiol puede proteger contra las lesiones cerebrales mediante la regulación de las fluctuaciones del calcio intracelular. Un estudio de noviembre de 2016 en la European Journal of Pharmacology encontró que un “desequilibrio de la homeostasis de sodio y calcio desencadenan procesos fisiopatológicos en la isquemia cerebral, que aceleran la muerte cerebral neuronal”. La buena noticia para las víctimas de accidente cerebrovascular, según científicos iraníes en Shahid Beheshti University en Teherán, es que el CBD puede reducir la gravedad del daño isquémico mediante el aumento de la expresión del receptor NCX en la membrana mitocondrial.
Regeneración incesante
Los cannabinoides promueven la neuroplasticidad y median la homeostasis a través de diversas vías bidireccionales. Consideremos, por ejemplo, el efecto bifásico del THC. Mientras que la mayoría de los fármacos siguen la tendencia de que una dosis más alta causa un efecto más fuerte, el THC y otros cannabinoides pueden accionar una respuesta bifásica de la dosis. Un efecto bifásico se refiere a dos respuestas opuestas a un solo compuesto; Esto no es infrecuente, especialmente entre los cannabinoides. Se ha demostrado que el THC aumenta la actividad mitocondrial en una dosis psicoactiva suave, mientras que la disminuye a dosis más altas4.
Las respuestas bifásicas a las dosis a menudo se producen cuando un compuesto influye en una célula a través de múltiples canales. Con respecto a la función mitocondrial, los efectos bifásicos de los cannabinoides dependen de las condiciones celulares, así como la dosificación. Por ejemplo, a altas dosis, el THC reducirá la actividad mitocondrial al unirse a receptores CB1 en la superficie del organelo; Pero a dosis bajas el THC puede causar un efecto opuesto al cambiar la fluidez de la membrana mitocondrial de manera que promueva la síntesis del trifosfato de adenosina (ATP) y la respiración celular. La fluidez y la permeabilidad de la membrana también son moduladas por otros factores epigenéticos, incluyendo diferentes niveles de colesterol y grasas dietarias.
Las acciones del CBD y el THC en las mitocondrias destacan algunas de las formas en que el sistema endocannabinoide regula la reparación y renovación celular. El estado predeterminado de nuestro cuerpo es uno de regeneración incesante. El cambio continuo a nivel celular es el punto de apoyo de la salud, la dinámica subyacente a la homeostasis. En tiempos de enfermedad, los procesos regenerativos son superados por disfunción y degradación. Los cannabinoides y otros antioxidantes penetrantes de membrana pueden mejorar la función mitocondrial y restaurar el equilibrio fisiológico.
Adrian Devitt-Lee es un investigador asociado a Project CBD. Derechos reservados, Project CBD. No debe ser reimpreso sin autorización.
Notas de pie
- La razón para el efecto Warburg, como se entiende hoy, es que las células cancerígenas necesitan materiales para sintetizar ADN, proteínas y la membrana celular. La necesidad de biomateriales es más significativa que la necesidad de energía. Si las mitocondrias no están activas, en su lugar ocurrirá una forma de fermentación. Esto produce una pequeña cantidad de energía pero deja las moléculas que pueden ser usadas como precursores de material celular.
- Una medida de estrés en una célula es la concentración de calcio citostólico (calcio en el espacio intracelular). El calcio es un mensajero secundario importante dentro de una célula; Modula la actividad e inhibición de diversas proteínas e influye en muchas señales celulares, incluyendo la apoptosis. A nivel celular, el calcio se almacena principalmente dentro de la mitocondria y otro organelo, el retículo endoplásmico.
- ¿Por qué los cannabinoides tienden a ser tóxicos en las células cancerosas, pero protectores en otros tipos de células? (Tenga en cuenta que esto es una tendencia, hay muchas excepciones.) Los regímenes de quimioterapia normalmente implican la generación de estrés oxidativo excesivo para precipitar la apoptosis. El CBD tiene potentes propiedades antitumorales, pero es un robusto antioxidante. Curiosamente, varios estudios sugieren que los antioxidantes mitocondriales específicos, como el CBD, trabajan sinérgicamente con los regímenes quimioterapéuticos convencionales para promover la muerte de las células cancerosas, aun cuando los antioxidantes típicamente interfieren con la quimioterapia. La combinación de cannabinoides vegetales y agentes quimioterapéuticos farmacéuticos ha sido examinada hasta cierto punto y es prometedora.
- Una dosis psicoactiva suave es 6,25 μM de THC, según se determinó por A. Athanasiou, et al (2007). Las altas dosis mencionadas son 10-100 μM de THC. Las dosis fisiológicas relevantes en seres humanos parecen estar alrededor de 1-20 μM de THC. Los estudios a menudo usan dosis muy altas porque los animales pequeños como los ratones tienen metabolismos mucho más rápidos, por lo que el fármaco se elimina de su sistema más rápido. Para contrarrestar esto, los científicos a veces dan una dosis muy alta, de tal manera que la dosis objetivo se alcanza en un cierto punto del tiempo (por ejemplo, 10 μM de THC a los 10 min). Esta es una de las muchas razones por las que la investigación preclínica no siempre se traduce en la experiencia humana con las drogas. El hecho de que las dosis pertinentes de THC están justo en la cúspide de su efecto bifásico es probablemente una de las muchas razones por las que la investigación con THC y la mitocondria es tan desafiante.
Fuentes
- Athanasiou A, Clarke AB, Turner AE, Kumaran NM, Vakilpour S, et al. Cannabinoid receptor agonists are mitochondrial inhibitors: a unified hypothesis of how cannabinoids modulate mitochondrial function and induce cell death. Biochem Biophys Res Commun. 2007 Dec 7;364(1):131-7.
- Bénard G, Massa F, Puente N, Lourenço J, Bellocchio L, et al. Mitochondrial CB₁ receptors regulate neuronal energy metabolism. Nat Neurosci. 2012 Mar 4;15(4):558-64.
- Bilkei-Gorzo A. The endocannabinoid system in normal and pathological brain ageing. Philos Trans R Soc Lond B Biol Sci. 2012 Dec 5;367(1607):3326-41.
- Fišar Z, Singh N, Hroudová J. Cannabinoid-induced changes in respiration of brain mitochondria. Toxicol Lett. 2014 Nov 18;231(1):62-71.
- Hao E, Mukhopadhyay P, Cao Z, Erdélyi K, Holovac E, et al. Cannabidiol Protects against Doxorubicin-Induced Cardiomyopathy by Modulating Mitochondrial Function and Biogenesis. Mol Med. 2015 Jan 6;21:38-45.
- Hebert-Chatelain E, Reguero L, Puente N, Lutz B, Chaouloff F, et al. Cannabinoid control of brain bioenergetics: Exploring the subcellular localization of the CB1 receptor. Mol Metab. 2014 Apr 2;3(4):495-504.
- Khaksar S, Bigdeli MR. Anti-excitotoxic effects of cannabidiol are partly mediated by enhancement of NCX2 and NCX3 expression in animal model of cerebral ischemia. Eur J Pharmacol. 2016 Nov 14;794:270-279.
- Ma L, Jia J, Niu W, Jiang T, Zhai Q, et al. Mitochondrial CB1 receptor is involved in ACEA-induced protective effects on neurons and mitochondrial functions. Sci Rep. 2015 Jul 28;5:12440.
- Mendizabal-Zubiaga J, Melser S, Bénard G, Ramos A, Reguero L, et al. Cannabinoid CB1 Receptors Are Localized in Striated Muscle Mitochondria and Regulate Mitochondrial Respiration. Front Physiol. 2016 Oct 25;7:476.
- Ryan D, Drysdale AJ, Lafourcade C, Pertwee RG, Platt B. Cannabidiol targets mitochondria to regulate intracellular Ca2+ levels. J Neurosci. 2009 Feb 18;29(7):2053-63.
- Samsel A, Seneff S. Glyphosate, pathways to modern diseases III: Manganese, neurological diseases, and associated pathologies. Surg Neurol Int. 2015 Mar 24;6:45.
- Shrivastava A, Kuzontkoski PM, Groopman JE, Prasad A. Cannabidiol induces programmed cell death in breast cancer cells by coordinating the cross-talk between apoptosis and autophagy. Mol Cancer Ther. 2011 Jul;10(7):1161-72.
- Singh N, Hroudová J, Fišar Z. Cannabinoid-Induced Changes in the Activity of Electron Transport Chain Complexes of Brain Mitochondria. J Mol Neurosci. 2015 Aug;56(4):926-31.
- Zaccagnino P, D’Oria S, Romano LL, Di Venere A, Sardanelli AM, et al. The endocannabinoid 2-arachidonoylglicerol decreases calcium induced cytochrome c release from liver mitochondria. J Bioenerg Biomembr. 2012 Apr;44(2):273-80.